Coordinación Regulatoria
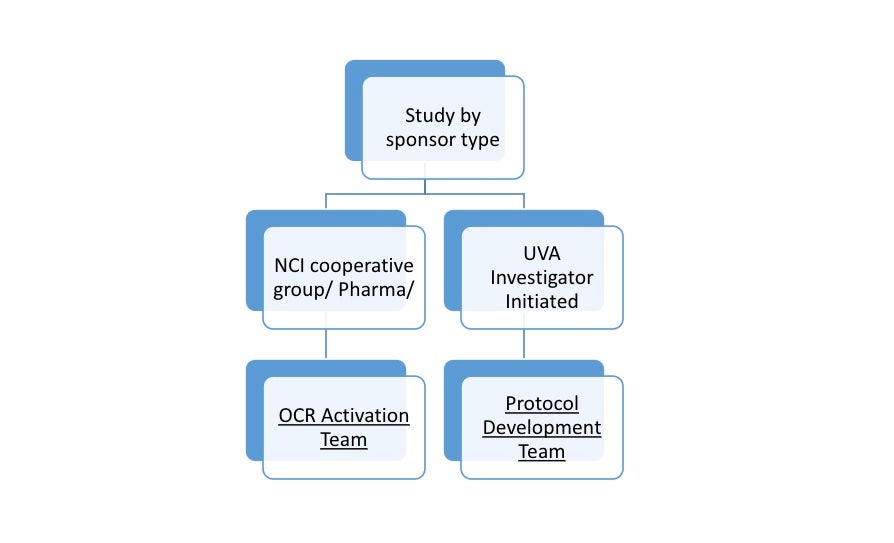
La Oficina de Investigación Clínica provee apoyo para toda necesaria sumisión regulatoria para estudios clínicos de cáncer realizados por grupos cooperativos, sean patrocinados por industria o por NCI, siempre que no sean iniciados por investigadores de UVA.
Ensayos clínicos iniciados por investigadores asociados con UVA reciben apoyo mediante el Equipo de Desarrollo de Protocolos.
El equipo regulatorio de la OIC se divide en dos grupos, y facilita las tareas obligatorias para ambos:
Este equipo es responsable de:
- Enrutamiento de CDA
- Visitas previas a la selección del sitio (PSV)
- Presentación regulatoria al PRC, IRB de registro, incluido el IRG-HSR de UVA o el IRB central, y otros comités internos
- Presentación de documentos esenciales del patrocinador y activación del estudio hasta la visita de Inicio del Sitio (SIV)
Para saber más, comuníquese con Eleanor Gorham, Gerente de Activación, eg3ap@uvahealth.org o 434-297-5726.
Este equipo es responsable de:
- Mantenimiento de enmiendas y otros aspectos regulatorios del estudio desde SIV hasta el cierre
- Archivado de materiales del estudio después del cierre
- Educación y comunicación para toda la documentación regulatoria requerida
- Seguimiento del entrenamiento CITI para todos los nuevos y actuales miembros de UVA NCTN
- Presentación de RCR al NCI para médicos nuevos y renovaciones para médicos existentes
Para saber más, comuníquese con Kirsten Bugden, Gerente de Normas, kb8wj@uvahealth.org o 434-243-7064.